因无菌工艺问题,Edge Pharma,LLC自愿召回所有药品
公司公告日期:2021年12月4日
FDA公开日期:2021年12月7日
产品类型:药品
公告原因:由于工艺问题无法保证无菌产品安全性和质量。
公司名称:Edge Pharma, LLC
品牌名:Edge Pharma, LLC
产品:Edge Pharma, LLC所有药品
公司公告
Edge Pharma, LLC自愿召回公司所有药品。由于工艺问题,公司无法保证达到无菌产品预期的无菌标准,考虑到产品的质量和安全性,现对所有药品进行召回。
风险承诺:使用未达到无菌标准的无菌药品,可导致特定部位感染和严重的全身感染,可能危及生命。迄今为止,Edge Pharma, LLC尚未收到任何与此次召回相关的不良事件。
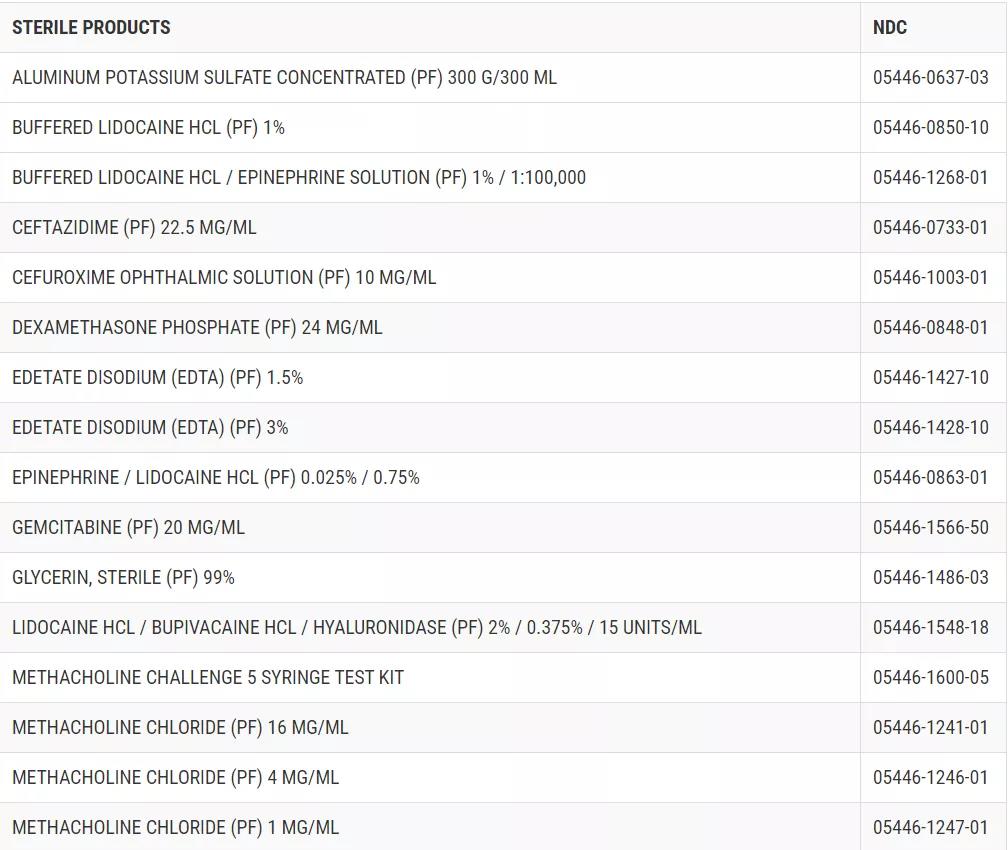
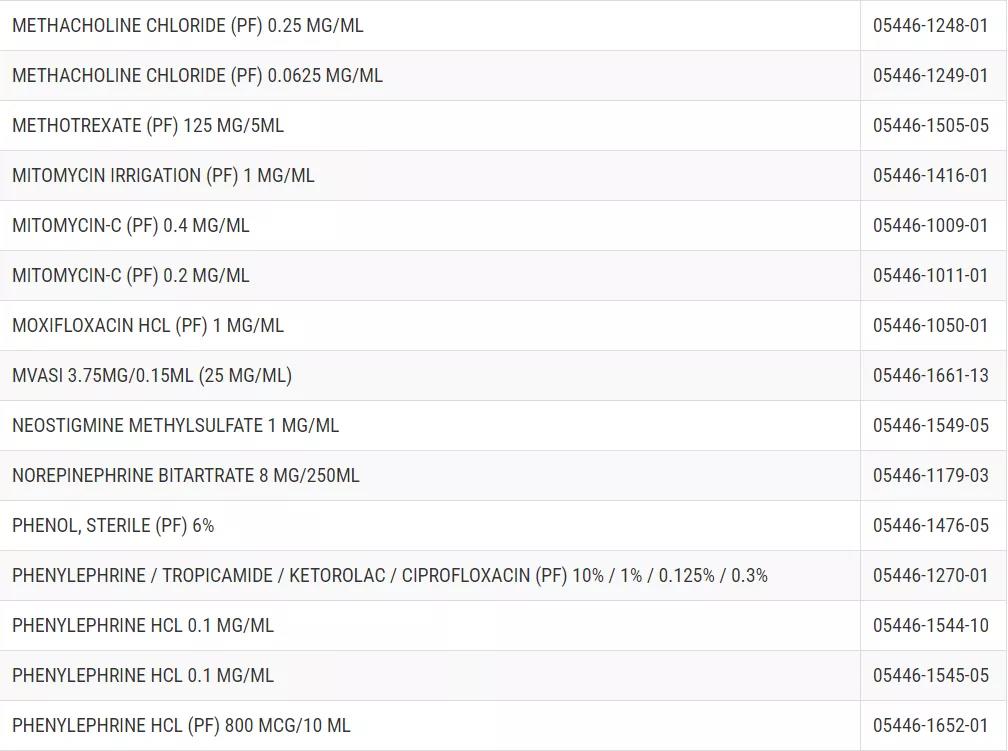
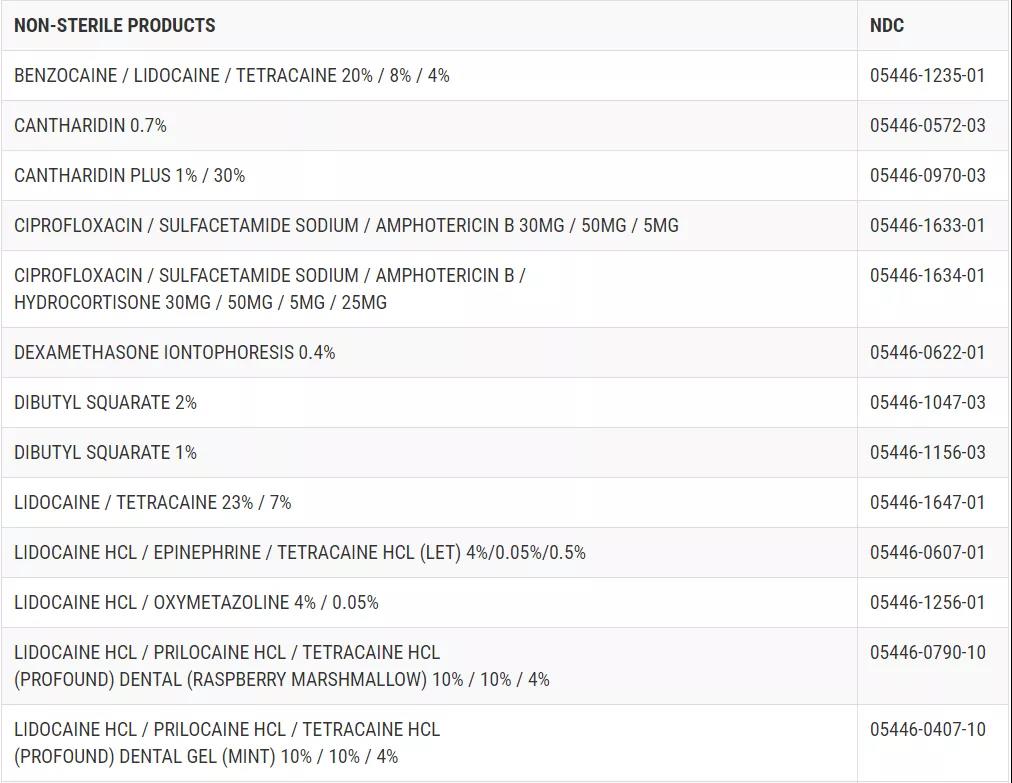
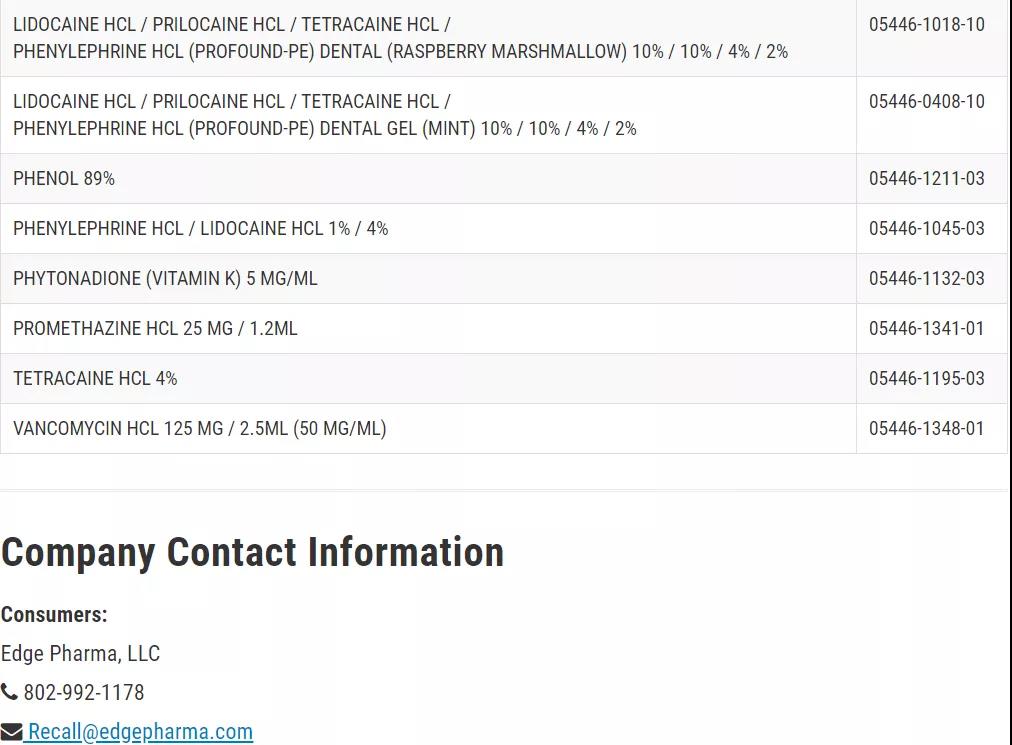
产品用于各种适应症,并包装在容器,静脉袋,注射器,滴注容器,小瓶,玻璃瓶和罐子。受影响批次及到期日见下方链接。药物的名称和浓度见下表。
关于批号、分发日期和药品信息的链接将于2021-12-08生效。
https://edgepharma.com/assets/recalledproducts.pdfExternal Link Disclaimer
此次召回包括所有由Edge Pharma, LLC分发的无菌和非无菌药品。此次召回的产品在全国范围内直接分发给客户或医疗机构。产品可通过具有Edge Pharma, LLC名称和标志的标签进行标识。
Edge Pharma, LLC正在通过电子邮件、媒体和FDA警报通知客户,并直接联系客户。持有 Edge Pharma, LLC此次召回批次产品的消费者和机构应立即停止使用产品,可选择退回或丢弃。
对此次召回有疑问的消费者可在美国东部时间周一至周五上午8点到下午4点通过电话号码或电子邮件地址联系Edge Pharma, LLC。如果消费者遇到了任何可能与服用或使用这些药物产品有关的问题,则应联系医生或医疗保健提供者。
在使用产品时遇到的不良反应或质量问题可通过在线、普通邮件或传真报告的方式递送至FDA MedWatch不良事件报告计划。
请在线完成并提交报告
邮件或传真:下载表格或拨打1-800-332-1088要求填写报告表格,然后填写并返回地址地址,或传真至1-800-FDA-0178
此次召回在美国食品和药物管理局的监管下进行。


关于Edge Pharma
Edge Pharma 是一家制药无菌和非无菌 503B 外包设施,为医疗保健社区提供高质量的创新解决方案。Edge 世界一流的科学、药学和工程人员了解您的组织(无论规模大小)正在应对的挑战。
据药融云数据库显示,Edge Pharma 共有11款药物已上市。
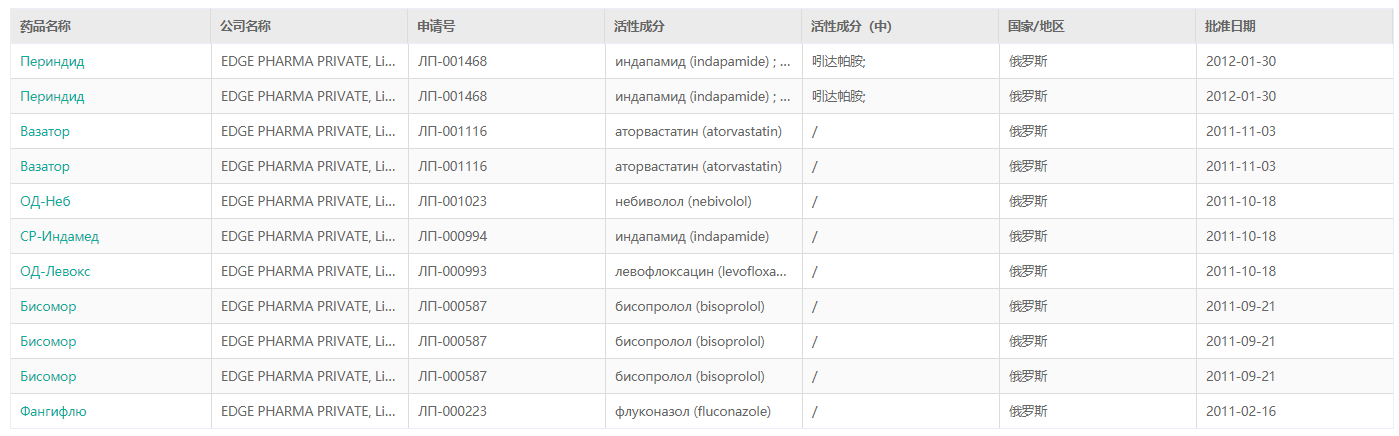
截图来源:药融云上市药品筛选数据库













































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论